Тест А6 Зависимость свойств веществ от их состава и строения. Физические свойства натрия на основе кристаллической решетки - урок с элементами модуля "кристаллическая решетка и ее виды" Зависимость свойств веществ от строения
Лекция 7Зависимость свойств веществ от их
строения. Химическая связь. Основные
виды химической связи.
Рассматриваемые вопросы:
1. Уровни организации вещества. Иерархия структуры.
2. Вещества молекулярного и немолекулярного строения.
3.
4. Причины возникновения химической связи.
5. Ковалентная связь: механизмы образования, способы
перекрывания атомных орбиталей, полярность, дипольный момент
молекулы.
6. Ионная связь.
7. Сравнение ковалентной полярной и ионной связи.
8. Сравнение свойств веществ с ковалентными полярными и
ионными связями.
9. Металлическая связь.
10. Межмолекулярные взаимодействия.Вещество (более 70 млн.)
Что надо знать о каждом веществе?
Формула (из чего состоит)
Структура (как устроено)
Физические свойства
Химические свойства
Способы получения
(лаб. и промышл.)
6. Практическое применение
1.
2.
3.
4.
5.Иерархия структуры вещества
Все вещества
состоят из
атомов, но не
все – из
молекул.
Атом
Молекула
У всех веществ
Только у веществ
молекулярного
строения
Наноуровень
У всех веществ
Объемный (макро)
уровень
У всех веществ
Все 4 уровня – объект изучения химииВещества молекулярного
и немолекулярного строенияВещества
Молекулярного
строения
Немолекулярного
строения
Состоят из молекул
Состоят из атомов
или ионов
H2O, CO2, HNO3, C60,
почти все орг. вещества
Алмаз, графит, SiO2,
металлы, соли
Формула отражает
состав молекулы
Формула отражает состав
формульной единицыВещества
Хлорид натрия
Формульная единица NaClВещества
Диоксид кремния
Формульная единица SiO2
Минералогический музей имени Ферсмана находится возле входа в Нескучный сад.
Адрес: Москва, Ленинский проспект, дом 18, корпус 2.Разнообразие химических структур.
пропеллан
C5H6
коронен
(супербензол)
C24H12
кавитанд
C36H32O8Разнообразие химических структур.
катенанРазнообразие химических структур.
катенанРазнообразие химических структур.
лист МебиусаМолекула
Молекула – устойчивая система, состоящая из нескольких
атомных ядер и электронов.
Атомы объединяются в молекулы путем образования
химических связей.
Главная движущая сила образования молекулы из
атомов – уменьшение общей энергии.
Молекулы имеют геометрическую форму, характеризующуюся
расстояниями между ядрами и углами между связями.Главная движущая сила
образования химической связи
между частицами вещества –
уменьшение общей энергии
системы.Основные типы химической
связи:
1.Ионная
2.Ковалентная
3.Металлическая
Основные межмолекулярные
взаимодействия:
1.Водородные связи
2.Ван-дер-Ваальсовы связиИонная связь
Если связь образуют атомы с резко различающимися
значениями электроотрицательности (ΔОЭО ≥ 1,7),
общая электронная пара практически полностью
смещается в сторону более электроотрицательного
атома.
Na Cl
ОЭО 0,9 3,16
∆ 2,26
+Na
Анион
:ClКатион
Химическая связь между ионами, возникающая за
счет их электростатического притяжения,
называется ионной.Ионная связь
Кулоновский потенциал сферически
симметричен, направлен во все стороны,
поэтому ионная связь ненаправлена.
Кулоновский потенциал не имеет
ограничений на количество
присоединяемых противоионов -
следовательно, ионная связь
ненасыщаема.Ионная связь
Соединения с ионным типом связи
твердые, хорошо растворимые в
полярных растворителях, имеют высокие
температуры плавления и кипения.Ионная связь
Кривая I: притяжение ионов, если
бы они представляли собой
точечные заряды.
Кривая II: отталкивание ядер в
случае сильного сближения ионов.
Кривая III: минимум энергии Е0 на
кривой соответствует
равновесному состоянию ионной
пары, при котором силы
притяжения электронов к ядрам
скомпенсированы силами
отталкивания ядер между собой на
расстоянии r0,Химическая связь в молекулах
Химическую связь в молекулах можно описать с
позиций двух методов:
- метода валентных связей, МВС
- метода молекулярных орбиталей, ММОМетод валентных связей
Теория Гейтлера-Лондона
Основные положения метода ВС:
1. Связь образуют два электрона с противоположными
спинами, при этом происходит перекрывание волновых
функций и увеличивается электронная плотность между
ядрами.
2. Связь локализована в направлении максимального
перекрывания Ψ-функций электронов. Чем сильнее
перекрывание, тем прочнее связь.
dсв - длина
связи;
Есв - энергия
связи.Образование молекулы водорода:
Н· + ·Н → Н:Н
При сближении двух атомов
возникают силы притяжения и
отталкивания:
1) притяжения: «электрон-ядро»
соседних атомов;
2) отталкивания: «ядро-ядро»,
«электрон-электрон» соседних
атомов.Образование молекулы водорода:
Молекулярное
двухэлектронное облако,
обладающее максимальной
электронной плотностью.Химическая связь, осуществляемая общими
электронными парами, называется ковалентной.
Общая электронная пара может образоваться двумя
способами:
1) в результате объединения двух непарных электронов:
2) в результате обобществления неподеленной
электронной пары одного атома (донора) и пустой
орбитали другого (акцептора).
Два механизма образования ковалентной связи:
обменный и донорно-акцепторный.
плотности связи происходит по линии,
соединяющей центры атомов (ядра), то такое
перекрывание называется σ-связью:Способы перекрывания атомных орбиталей при
образовании ковалентной связи
Если образование максимальной электронной
плотности связи происходит по обе стороны
линии, соединяющей центры атомов (ядра), то
такое перекрывание называется π-связью:Полярная и неполярная ковалентная связь
1) Если связь образуют одинаковые атомы,
двухэлектронное облако связи распределяется в
пространстве симметрично между их ядрами - такая
связь называется неполярной: H2, Cl2, N2.
2) если связь образуют разные атомы, облако связи
смещено в сторону более электроотрицательного атома
- такая связь называется полярной: HCl, NH3, CO2.Полярная ковалентная связь
Дипольный момент связи
Диполь
H+δCl-δ или H+0,18Cl-0,18
Где ±δ - эффективный
заряд атома, доля
абсолютного заряда
электрона.
+δ
-δ
Не путать со степенью окисления!
l
Произведение эффективного заряда на длину диполя
называется электрическим моментом диполя: μ = δl
Это векторная величина: направлен от положительного
заряда к отрицательному.Полярная ковалентная связь
Дипольный момент молекулы
Дипольный момент молекулы равен сумме
векторов дипольных моментов связей с учетом
неподеленных электронных пар.
Единицей измерения дипольного момента
является Дебай: 1D = 3,3·10-30 Кл·м.Полярная ковалентная связь
Дипольный момент молекулы
В произведении μ = δl обе величины разнонаправлены.
Поэтому надо внимательно отслеживать причину
изменения μ.
Например,
CsF
CsCl
24
31
δ «проиграл» l
CsI
HF
HCl
HBr
HI
37
5,73
3,24
2,97
1,14
наоборотПолярная ковалентная связь
Дипольный момент молекулы
Может ли молекула быть неполярной, если
все связи в ней полярные?
Молекулы типа АВ всегда полярны.
Молекулы типа АВ2 могут быть и полярными, и
неполярными...
Н2О
О
Н
СО2
μ>0
Н
О
С
μ=0
ОПолярная ковалентная связь
Молекулы, состоящие из трех атомов и более
(АВ2, АВ3, АВ4, АВ5, АВ6) ,
могут быть неполярными, если они симметричны.
На что влияет наличие дипольного момента
молекулы?
Имеются межмолекулярные взаимодействия, а,
следовательно, увеличиваются плотность вещества,
t°плавления и t°кипения.Сравнение ионной и ковалентной полярной связей
Общее: образование общей
электронной пары.
Отличие: степень
смещения общей
электронной пары
(поляризация связи).
Ионную связь следует рассматривать как крайний
случай ковалентной полярной связи.
полярной связей
Ковалентная связь: насыщена и направлена
Насыщаемость (максимальная валентность) -
определяется способностью атома образовывать
ограниченное количество связей (с учетом обоих
механизмов образования).
Направление связи задает валентный угол, зависящий от
типа гибридизации орбиталей центрального атома.
Ионная связь: ненасыщена и ненаправлена.Сравнение характеристик ионной и ковалентной
полярной связей
Направленность связи задают валентные углы.
Валентные углы определяют экспериментально или
предсказывают на основе теории гибридизации
атомных орбиталей Л. Поллинга либо теории
Гиллеспи.
Подробно об этом на семинарах.
ковалентными связями
Ковалентные связи
Атомные кристаллы
Между атомами
в самом кристалле
Высокая твердость
высокие tºплав, tºкип
плохие тепло- и
электропроводность
Молекулярные кристаллы
Между атомами
в молекуле
Умеренная мягкость
достаточно низкие
tºплав, tºкип
плохие тепло- и
Электропроводность
Нерастворимы в водеСравнение свойств веществ с ионными и
ковалентными связями
Молекулярный кристалл
Температура плавления 112,85 °ССравнение свойств веществ с ионными и
ковалентными связями
Атомный ковалентный кристалл
Температура плавления ≈ 3700 °ССравнение свойств веществ с ионными и
ковалентными связями
Ионные связи
между ионами
в кристалле
твердость и хрупкость
высокая температура плавления
плохие тепло- и электропроводность
Растворимы в водеСравнение свойств веществ с ионными и
ковалентными связями
Ионный кристалл
Температура плавления ≈ 800 °СМеталлическая связь
Металлическая связь осуществляется электронами,
принадлежащими всем атомам одновременно.
Электронная плотность
делокализована «электронный газ».
Характерный
металлический блеск
Пластичность
Ковкость
Высокие тепло- и
электропроводность
Температуры плавления
очень разные.Межмолекулярные связи.
1. Водородная связь
Притяжение между атомом водорода (+) одной
молекулы и атомом F, O, N (–) другой молекулы
F
F
H
H
H
H
F
F
O
H3C
H
F
C
H
Полимер
(HF)n
O
C
O
H
CH3
Димер
уксусной кислоты
O
Водородные связи слабы индивидуально,
но сильны коллективноМежмолекулярные связи.
2. Водородная связь в ДНКМежмолекулярные связи.
3. Водородные связи в воде
жидкая вода
ледМежмолекулярные связи.
4. Образование водородных связей в
воде
жидкая вода
превращение
воды в ледМежмолекулярные связи.
5. Ван-дер-ваальсовы связи
Даже если между молекулами нет водородных связей,
молекулы всегда притягиваются друг к другу.
Притяжение между молекулярными диполями называют вандер-ваальсовой связью.
В-д-в притяжение тем сильнее, чем больше:
1) полярность; 2) размер молекул.
Пример: метан (CH4) – газ, бензол (C6H6) – жидкость
Одна из самых слабых в-д-в связей – между молекулами
H2 (т. пл. –259 оС, т. кип. –253 оС).
Взаимодействие между молекулами во много раз слабее связи между атомами:
Eков(Cl–Cl) = 244 кДж/моль, Eвдв(Cl2–Cl2) = 25 кДж/моль
но именно оно обеспечивает существование жидкого и твердого состояния веществаВ лекции использованы материалы профессора
химического факультета МГУ им. Ломоносова
Еремина Вадима Владимировича
Спасибо
за внимание!
Темы кодификатора ЕГЭ: Вещества молекулярного и немолекулярного строения. Тип кристаллической решетки. Зависимость свойств веществ от их состава и строения.
Молекулярно-кинетическая теория
Все молекулы состоят из мельчайших частиц – атомов. Все открытые на настоящий момент атомы собраны в таблице Менделеева.
Атом – это мельчайшая, химически неделимая частица вещества, сохраняющая его химические свойства. Атомы соединяются между собой химическими связями . Ранее мы уже рассматривали а. Обязательно озучите теорию по теме: Типы химических связей, перед тем, как изучать эту статью!
Теперь рассмотрим, как могут соединяться частицы в веществе.
В зависимости от расположения частиц друг относительно друга свойства образуемых ими веществ могут очень сильно различаться. Так, если частицы расположены друг от друга далеко (расстояние между частицами намного больше размеров самих частиц), между собой практически не взаимодействуют, перемещаются в пространстве хаотично и непрерывно, то мы имеем дело с газом .
Если частицы расположены близко друг к другу, но хаотично , больше взаимодействуют между собой , совершают интенсивные колебательные движения в одном положении, но могут перескакивать в другое положение, то это модель строения жидкости .
Если же частицы расположены близко к друг другу, но более упорядоченно , и больше взаимодействуют между собой, а двигаются только в пределах одного положения равновесия, практически не перемещаясь в другиеположения, то мы имеем дело с твердым веществом .

Большинство известных химических веществ и смесей могут существовать в твердом, жидком и газообразном состояниях. Самый простой пример – это вода . При нормальных условиях она жидкая , при 0 о С она замерзает – переходит из жидкого состояния в твердое , и при 100 о С закипает – переходит в газовую фазу – водяной пар. При этом многие вещества при нормальных условиях – газы, жидкости или твердые. Например, воздух – смесь азота и кислорода – это газ при нормальных условиях. Но при высоком давлении и низкой температуре азот и кислород конденсируются и переходят в жидкую фазу. Жидкий азот активно используют в промышленности. Иногда выделяют плазму , а также жидкие кристаллы, как отдельные фазы.

Очень многие свойства индивидуальных веществ и смесей объясняются взаимным расположением частиц в пространстве друг относительно друга!
Данная статья рассматривает свойства твердых тел , в зависимости от их строения. Основные физические свойства твердых веществ: температура плавления, электропроводность, теплопроводность, механическая прочность, пластичность и др.
Температура плавления – это такая температура, при которой вещество переходит из твердой фазы в жидкую, и наоборот.

– это способность вещества деформироваться без разрушения.

Электропроводность – это способность вещества проводить ток.
Ток – это упорядоченное движение заряженных частиц . Таким образом, ток могут проводить только такие вещества, в которых присутствуют подвижные заряженные частицы . По способности проводить ток вещества делят на проводники и диэлектрики. Проводники – это вещества, которые могут проводить ток (т.е. содержат подвижные заряженные частицы). Диэлектрики – это вещества, которые практически не проводят ток.

В твердом веществе частицы вещества могут располагаться хаотично , либо более упорядоченн о. Если частицы твердого вещества расположены в пространстве хаотично , вещество называют аморфным . Примеры аморфных веществ – уголь, слюдяное стекло .

Если частицы твердого вещества расположены в пространстве упорядоченно, т.е. образуют повторяющиеся трехмерные геометрические структуры, такое вещество называют кристаллом , а саму структуру – кристаллической решеткой . Большинство известных нам веществ – кристаллы. Сами частицы при этом расположены в узлах кристаллической решетки.
Кристаллические вещества различают, в частности, по типу химической связи между частицами в кристалле – атомные, молекулярные, металлические, ионные; по геометрической форме простейшей ячейки кристаллической решетки – кубическая, гексагональная и др.
В зависимости от типа частиц, образующих кристаллическую решетку , различают атомную, молекулярную, ионную и металлическую кристаллическую структуру .
Атомная кристаллическая решетка

Атомная кристаллическая решетка образуется, когда в узлах кристалла расположены атомы . Атомы соединены между собой прочными ковалентными химическими связями . Соответственно, такая кристаллическая решетка будет очень прочной , разрушить ее непросто. Атомную кристаллическую решетку могут образовывать атомы с высокой валентностью, т.е. с большим числом связей с соседними атомами (4 или больше). Как правило, это неметаллы: простые вещества — кремния, бора, углерода (аллотропные модификации алмаз, графит), и их соединения (бороуглерод, оксид кремния (IV) и др .). Поскольку между неметаллами возникает преимущественно ковалентная химическая связь, свободных электронов (как и других заряженных частиц) в веществах с атомной кристаллической решеткой в большинстве случаев нет . Следовательно, такие вещества, как правило, очень плохо проводят электрический ток, т.е. являются диэлектриками . Это общие закономерности, из которых есть ряд исключений.

Связь между частицами в атомных кристалалах: .
В узлах кристалла с атомной кристаллической структурой расположены атомы .
Фазовое состояние атомных кристаллов при нормальных условиях: как правило, твердые вещества .
Вещества , образующие в твердом состоянии атомные кристаллы:
- Простые вещества с высокой валентностью (расположены в середине таблицы Менделеева): бор, углерод, кремний, и др.
- Сложные вещества, образованные этими неметаллами: кремнезем (оксид кремния, кварцевый песок) SiO 2 ; карбид кремния (корунд) SiC; карбид бора, нитрид бора и др.
Физические свойства веществ с атомной кристаллической решеткой:
— прочность;
— тугоплавкость (высокая температура плавления);
— низкая электропроводность;
— низкая теплопроводность;
— химическая инертность (неактивные вещества);
— нерастворимость в растворителях.

Молекулярная кристаллическая решетка – это такая решетка, в узлах которой располагаются молекулы . Удерживают молекулы в кристалле слабые силы межмолекулярного притяжения (силы Ван-дер-Ваальса , водродные связи, или электростатическое притяжение). Соответственно, такую кристаллическую решетку, как правило, довольно легко разрушить . Вещества с молекулярной кристаллической решеткой – легкоплавкие, непрочные . Чем больше сила притяжения между молекулами, тем выше температура плавления вещества . Как правило, температуры плавления веществ с молекулярной кристаллической решеткой не выше 200-300К. Поэтому при нормальных условиях большинство веществ с молекулярной кристаллической решеткой существует в виде газов или жидкостей . Молекулярную кристаллическую решетку, как правило, образуют в твердом виде кислоты, оксиды неметаллов, прочие бинарные соединения неметаллов, простые вещества, образующие устойчивые молекулы (кислород О 2 , азот N 2 , вода H 2 O и др.), органические вещества. Как правило, это вещества с ковалентной полярной (реже неполярной) связью. Т.к. электроны задействованы в химических связях, вещества с молекулярной кристаллической решеткой – диэлектрики, плохо проводят тепло .

Связь между частицами в молекулярных кристалалах: межмолекулярные , электростатические или межмолекулярные силы притяжения .
В узлах кристалла с молекулярной кристаллической структурой расположены молекулы .
Фазовое состояние молекулярных кристаллов при нормальных условиях: газы, жидкости и твердые вещества .
Вещества , образующие в твердом состоянии молекулярные кристаллы :
- Простые вещества-неметаллы, образующие маленькие прочные молекулы (O 2 , N 2 , H 2 , S 8 и др.);
- Сложные вещества (соединения неметаллов) с ковалентными полярными связями (кроме оксидов кремния и бора, соединений кремния и углерода) — вода H 2 O, оксид серы SO 3 и др.
- Одноатомные инертные газы (гелий, неон, аргон, криптон и др.) ;
- Большинство органических веществ, в которых нет ионных связей — метан CH 4 , бензол С 6 Н 6 и др.
Физические свойства веществ с молекулярной кристаллической решеткой:
— легкоплавкость (низкая температура плавления):
— высокая сжимаемость;
— молекулярные кристаллы в твердом виде, а также в растворах и расплавах не проводят ток;
— фазовое состояние при нормальных условиях – газы, жидкости, твердые вещества;
— высокая летучесть;
— малая твердость.
Ионная кристаллическая решетка

В случае, если в узлах кристалла находятся заряженные частицы – ионы , мы можем говорить о ионной кристаллической решетке . Как правило, с ионных кристаллах чередуются положительные ионы (катионы) и отрицательные ионы (анионы), поэтому частицы в кристалле удерживаются силами электростатического притяжения . В зависимости от типа кристалла и типа ионов, образующих кристалл, такие вещества могут быть довольно прочными и тугоплавкими . В твердом состоянии подвижных заряженных частиц в ионных кристаллах, как правило, нет. Зато при растворении или расплавлении кристалла ионы высвобождаются и могут двигаться под действием внешнего электрического поля. Т.е. проводят ток только растворы или расплавы ионных кристаллов. Ионная кристаллическая решетка характерна для веществ с ионной химической связью . Примеры таких веществ – поваренная соль NaCl, карбонат кальция – CaCO 3 и др. Ионную кристаллическую решетку, как правило, в твердой фазе образуют соли, основания, а также оксиды металлов и бинарные соединения металлов и неметаллов .

Связь между частицами в ионных кристаллах: .
В узлах кристалла с ионной решеткой расположены ионы .
Фазовое состояние ионных кристаллов при нормальных условиях: как правило, твердые вещества .
Химические вещества с ионной кристаллической решеткой:
- Соли (органические и неорганические), в том числе соли аммония (например, хлорид аммония NH 4 Cl);
- Основания;
- Оксиды металлов;
- Бинарные соединения, в составе которых есть металлы и неметаллы.
Физические свойства веществ с ионной кристаллической структурой:
— высокая температура плавления (тугоплавкость);
— растворы и расплавы ионных кристаллов – проводники тока;
— большинство соединений растворимы в полярных растворителях (вода);
— твердое фазовое состояние у большинства соединений при нормальных условиях.

И, наконец, металлы характеризуются особым видом пространственной структуры – металлической кристаллической решеткой , которая обусловлена металлической химической связью . Атомы металлов довольно слабо удерживают валентные электроны. В кристалле, образованном металлом, происходят одновременно следующие процессы: часть атомов отдает электроны и становится положительно заряженными ионами ; эти электроны хаотично перемещаются в кристалле ; часть электронов притягивается к ионам . Эти процессы происходят одновременно и хаотично. Таким образом, возникают ионы , как при образовании ионной связи, и образуются общие электроны , как при образовании ковалентной связи. Свободные электроны перемещаются хаотично и непрерывно по всему объему кристалла, как газ. Поэтому иногда их называют «электронным газом ». Из-за наличия большого числа подвижных заряженных частиц металлы проводят ток, тепло . Температура плавления металлов сильно варьируется. Металлы также характеризуются своеобразным металлическим блеском, ковкостью , т.е. способностью изменять форму без разрушения при сильном механическом воздействии, т.к. химические связи при этом не разрушаются.

Связь между частицами : .
В узлах кристалла с металлической решеткой расположены ионы металлов и атомы .
Фазовое состояние металлов при обычных условиях: как правило, твердые вещества (исключение — ртуть, жидкость при обычных условиях).
Химические вещества с металлической кристаллической решеткой — простые вещества-металлы .
Физические свойства веществ с металлической кристаллической решеткой:
— высокая тепло- и электропроводность;
— ковкость и пластичность;
— металлический блеск;
— металлы, как правило, нерастворимы в растворителях;
— большинство металлов – твердые вещества при нормальных условиях.
Сравнение свойств веществ с различными кристаллическими решетками
Тип кристаллической решетки (или отсутствие кристаллической решетки) позволяет оценить основные физические свойства вещества . Для примерного сравнения типичных физических свойств соединений с разными кристаллическими решетками очень удобно использовать химические вещества с характерными свойствами . Для молекулярной решетки это, например, углекислый газ , для атомной кристаллической решетки — алмаз , для металлической — медь , и для ионной кристаллической решетки — поваренная соль , хлорид натрия NaCl.

Сводная таблица по структурам простых веществ, образованных химическими элементами из главных подгрупп таблицы Менделеева (элементы побочных подгрупп являются металлами, следовательно, имеют металлическую кристаллическую решетку).

Итоговая таблица связи свойств веществ со строением:

Лекция 7 Зависимость свойств веществ от их строения. Химическая связь. Основные виды химической связи. Рассматриваемые вопросы: 1. Уровни организации вещества. Иерархия структуры. 2. Вещества молекулярного и немолекулярного строения. 3. Разнообразие химических структур. 4. Причины возникновения химической связи. 5. Ковалентная связь: механизмы образования, способы перекрывания атомных орбиталей, полярность, дипольный момент молекулы. 6. Ионная связь. 7. Сравнение ковалентной полярной и ионной связи. 8. Сравнение свойств веществ с ковалентными полярными и ионными связями. 9. Металлическая связь. 10. Межмолекулярные взаимодействия.
 Вещество (более 70 млн.) Что надо знать о каждом веществе? 1. 2. 3. 4. 5. Формула (из чего состоит) Структура (как устроено) Физические свойства Химические свойства Способы получения (лаб. и промышл.) 6. Практическое применение
Вещество (более 70 млн.) Что надо знать о каждом веществе? 1. 2. 3. 4. 5. Формула (из чего состоит) Структура (как устроено) Физические свойства Химические свойства Способы получения (лаб. и промышл.) 6. Практическое применение
 Иерархия структуры вещества Все вещества состоят из атомов, но не все – из молекул. Атом Молекула У всех веществ Только у веществ молекулярного строения Наноуровень У всех веществ Объемный (макро) уровень У всех веществ Все 4 уровня – объект изучения химии
Иерархия структуры вещества Все вещества состоят из атомов, но не все – из молекул. Атом Молекула У всех веществ Только у веществ молекулярного строения Наноуровень У всех веществ Объемный (макро) уровень У всех веществ Все 4 уровня – объект изучения химии
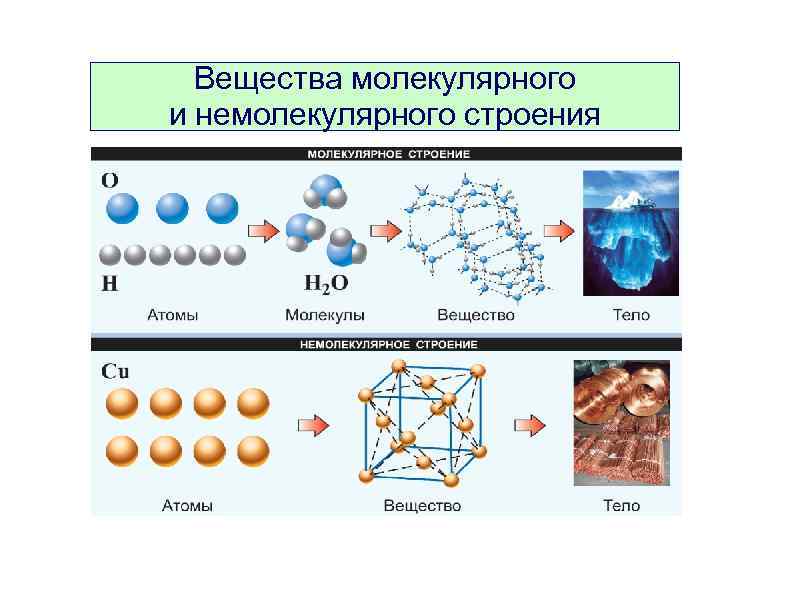
 Вещества Молекулярного строения Немолекулярного строения Состоят из молекул Состоят из атомов или ионов H 2 O, CO 2, HNO 3, C 60, почти все орг. вещества Алмаз, графит, Si. O 2, металлы, соли Формула отражает состав молекулы Формула отражает состав формульной единицы
Вещества Молекулярного строения Немолекулярного строения Состоят из молекул Состоят из атомов или ионов H 2 O, CO 2, HNO 3, C 60, почти все орг. вещества Алмаз, графит, Si. O 2, металлы, соли Формула отражает состав молекулы Формула отражает состав формульной единицы

 Вещества Диоксид кремния Формульная единица Si. O 2 Минералогический музей имени Ферсмана находится возле входа в Нескучный сад. Адрес: Москва, Ленинский проспект, дом 18, корпус 2.
Вещества Диоксид кремния Формульная единица Si. O 2 Минералогический музей имени Ферсмана находится возле входа в Нескучный сад. Адрес: Москва, Ленинский проспект, дом 18, корпус 2.
 Разнообразие химических структур. пропеллан C 5 H 6 коронен (супербензол) C 24 H 12 кавитанд C 36 H 32 O 8
Разнообразие химических структур. пропеллан C 5 H 6 коронен (супербензол) C 24 H 12 кавитанд C 36 H 32 O 8



 Молекула – устойчивая система, состоящая из нескольких атомных ядер и электронов. Атомы объединяются в молекулы путем образования химических связей. Главная движущая сила образования молекулы из атомов – уменьшение общей энергии. Молекулы имеют геометрическую форму, характеризующуюся расстояниями между ядрами и углами между связями.
Молекула – устойчивая система, состоящая из нескольких атомных ядер и электронов. Атомы объединяются в молекулы путем образования химических связей. Главная движущая сила образования молекулы из атомов – уменьшение общей энергии. Молекулы имеют геометрическую форму, характеризующуюся расстояниями между ядрами и углами между связями.

 Основные типы химической связи: 1. Ионная 2. Ковалентная 3. Металлическая Основные межмолекулярные взаимодействия: 1. Водородные связи 2. Ван-дер-Ваальсовы связи
Основные типы химической связи: 1. Ионная 2. Ковалентная 3. Металлическая Основные межмолекулярные взаимодействия: 1. Водородные связи 2. Ван-дер-Ваальсовы связи
 Ионная связь Если связь образуют атомы с резко различающимися значениями электроотрицательности (ΔОЭО ≥ 1, 7), общая электронная пара практически полностью смещается в сторону более электроотрицательного атома. Na Cl ОЭО 0, 9 3, 16 ∆ 2, 26 +Na Анион: Cl. Катион Химическая связь между ионами, возникающая за счет их электростатического притяжения, называется ионной.
Ионная связь Если связь образуют атомы с резко различающимися значениями электроотрицательности (ΔОЭО ≥ 1, 7), общая электронная пара практически полностью смещается в сторону более электроотрицательного атома. Na Cl ОЭО 0, 9 3, 16 ∆ 2, 26 +Na Анион: Cl. Катион Химическая связь между ионами, возникающая за счет их электростатического притяжения, называется ионной.
 Ионная связь Кулоновский потенциал сферически симметричен, направлен во все стороны, поэтому ионная связь ненаправлена. Кулоновский потенциал не имеет ограничений на количество присоединяемых противоионов - следовательно, ионная связь ненасыщаема.
Ионная связь Кулоновский потенциал сферически симметричен, направлен во все стороны, поэтому ионная связь ненаправлена. Кулоновский потенциал не имеет ограничений на количество присоединяемых противоионов - следовательно, ионная связь ненасыщаема.
 Ионная связь Соединения с ионным типом связи твердые, хорошо растворимые в полярных растворителях, имеют высокие температуры плавления и кипения.
Ионная связь Соединения с ионным типом связи твердые, хорошо растворимые в полярных растворителях, имеют высокие температуры плавления и кипения.
 Ионная связь Кривая I: притяжение ионов, если бы они представляли собой точечные заряды. Кривая II: отталкивание ядер в случае сильного сближения ионов. Кривая III: минимум энергии Е 0 на кривой соответствует равновесному состоянию ионной пары, при котором силы притяжения электронов к ядрам скомпенсированы силами отталкивания ядер между собой на расстоянии r 0,
Ионная связь Кривая I: притяжение ионов, если бы они представляли собой точечные заряды. Кривая II: отталкивание ядер в случае сильного сближения ионов. Кривая III: минимум энергии Е 0 на кривой соответствует равновесному состоянию ионной пары, при котором силы притяжения электронов к ядрам скомпенсированы силами отталкивания ядер между собой на расстоянии r 0,
 Химическая связь в молекулах Химическую связь в молекулах можно описать с позиций двух методов: - метода валентных связей, МВС - метода молекулярных орбиталей, ММО
Химическая связь в молекулах Химическую связь в молекулах можно описать с позиций двух методов: - метода валентных связей, МВС - метода молекулярных орбиталей, ММО
 Метод валентных связей Теория Гейтлера-Лондона Основные положения метода ВС: 1. Связь образуют два электрона с противоположными спинами, при этом происходит перекрывание волновых функций и увеличивается электронная плотность между ядрами. 2. Связь локализована в направлении максимального перекрывания Ψ-функций электронов. Чем сильнее перекрывание, тем прочнее связь.
Метод валентных связей Теория Гейтлера-Лондона Основные положения метода ВС: 1. Связь образуют два электрона с противоположными спинами, при этом происходит перекрывание волновых функций и увеличивается электронная плотность между ядрами. 2. Связь локализована в направлении максимального перекрывания Ψ-функций электронов. Чем сильнее перекрывание, тем прочнее связь.

 Образование молекулы водорода: Н· + ·Н → Н: Н При сближении двух атомов возникают силы притяжения и отталкивания: 1) притяжения: «электрон-ядро» соседних атомов; 2) отталкивания: «ядро-ядро» , «электрон-электрон» соседних атомов.
Образование молекулы водорода: Н· + ·Н → Н: Н При сближении двух атомов возникают силы притяжения и отталкивания: 1) притяжения: «электрон-ядро» соседних атомов; 2) отталкивания: «ядро-ядро» , «электрон-электрон» соседних атомов.

 Химическая связь, осуществляемая общими электронными парами, называется ковалентной. Общая электронная пара может образоваться двумя способами: 1) в результате объединения двух непарных электронов: 2) в результате обобществления неподеленной электронной пары одного атома (донора) и пустой орбитали другого (акцептора). Два механизма образования ковалентной связи: обменный и донорно-акцепторный.
Химическая связь, осуществляемая общими электронными парами, называется ковалентной. Общая электронная пара может образоваться двумя способами: 1) в результате объединения двух непарных электронов: 2) в результате обобществления неподеленной электронной пары одного атома (донора) и пустой орбитали другого (акцептора). Два механизма образования ковалентной связи: обменный и донорно-акцепторный.
 Способы перекрывания атомных орбиталей при образовании ковалентной связи Если образование максимальной электронной плотности связи происходит по линии, соединяющей центры атомов (ядра), то такое перекрывание называется σ-связью:
Способы перекрывания атомных орбиталей при образовании ковалентной связи Если образование максимальной электронной плотности связи происходит по линии, соединяющей центры атомов (ядра), то такое перекрывание называется σ-связью:
 Способы перекрывания атомных орбиталей при образовании ковалентной связи Если образование максимальной электронной плотности связи происходит по обе стороны линии, соединяющей центры атомов (ядра), то такое перекрывание называется π-связью:
Способы перекрывания атомных орбиталей при образовании ковалентной связи Если образование максимальной электронной плотности связи происходит по обе стороны линии, соединяющей центры атомов (ядра), то такое перекрывание называется π-связью:
 Полярная и неполярная ковалентная связь 1) Если связь образуют одинаковые атомы, двухэлектронное облако связи распределяется в пространстве симметрично между их ядрами - такая связь называется неполярной: H 2, Cl 2, N 2. 2) если связь образуют разные атомы, облако связи смещено в сторону более электроотрицательного атома - такая связь называется полярной: HCl, NH 3, CO 2.
Полярная и неполярная ковалентная связь 1) Если связь образуют одинаковые атомы, двухэлектронное облако связи распределяется в пространстве симметрично между их ядрами - такая связь называется неполярной: H 2, Cl 2, N 2. 2) если связь образуют разные атомы, облако связи смещено в сторону более электроотрицательного атома - такая связь называется полярной: HCl, NH 3, CO 2.
 Полярная ковалентная связь Дипольный момент связи Диполь H+δCl-δ или H+0, 18 Cl-0, 18 +δ -δ Где ±δ - эффективный заряд атома, доля абсолютного заряда электрона. Не путать со степенью окисления! l Произведение эффективного заряда на длину диполя называется электрическим моментом диполя: μ = δl Это векторная величина: направлен от положительного заряда к отрицательному.
Полярная ковалентная связь Дипольный момент связи Диполь H+δCl-δ или H+0, 18 Cl-0, 18 +δ -δ Где ±δ - эффективный заряд атома, доля абсолютного заряда электрона. Не путать со степенью окисления! l Произведение эффективного заряда на длину диполя называется электрическим моментом диполя: μ = δl Это векторная величина: направлен от положительного заряда к отрицательному.
 Полярная ковалентная связь Дипольный момент молекулы равен сумме векторов дипольных моментов связей с учетом неподеленных электронных пар. Единицей измерения дипольного момента является Дебай: 1 D = 3, 3· 10 -30 Кл·м.
Полярная ковалентная связь Дипольный момент молекулы равен сумме векторов дипольных моментов связей с учетом неподеленных электронных пар. Единицей измерения дипольного момента является Дебай: 1 D = 3, 3· 10 -30 Кл·м.
 Полярная ковалентная связь Дипольный момент молекулы В произведении μ = δl обе величины разнонаправлены. Поэтому надо внимательно отслеживать причину изменения μ. Например, Cs. F Cs. Cl 24 31 δ «проиграл» l Cs. I HF HCl HBr HI 37 5, 73 3, 24 2, 97 1, 14 наоборот
Полярная ковалентная связь Дипольный момент молекулы В произведении μ = δl обе величины разнонаправлены. Поэтому надо внимательно отслеживать причину изменения μ. Например, Cs. F Cs. Cl 24 31 δ «проиграл» l Cs. I HF HCl HBr HI 37 5, 73 3, 24 2, 97 1, 14 наоборот
 Полярная ковалентная связь Дипольный момент молекулы Может ли молекула быть неполярной, если все связи в ней полярные? Молекулы типа АВ всегда полярны. Молекулы типа АВ 2 могут быть и полярными, и неполярными. . . Н 2 О О Н СО 2 μ>0 Н О С μ=0 О
Полярная ковалентная связь Дипольный момент молекулы Может ли молекула быть неполярной, если все связи в ней полярные? Молекулы типа АВ всегда полярны. Молекулы типа АВ 2 могут быть и полярными, и неполярными. . . Н 2 О О Н СО 2 μ>0 Н О С μ=0 О
 Полярная ковалентная связь Молекулы, состоящие из трех атомов и более (АВ 2, АВ 3, АВ 4, АВ 5, АВ 6) , могут быть неполярными, если они симметричны. На что влияет наличие дипольного момента молекулы? Имеются межмолекулярные взаимодействия, а, следовательно, увеличиваются плотность вещества, t°плавления и t°кипения.
Полярная ковалентная связь Молекулы, состоящие из трех атомов и более (АВ 2, АВ 3, АВ 4, АВ 5, АВ 6) , могут быть неполярными, если они симметричны. На что влияет наличие дипольного момента молекулы? Имеются межмолекулярные взаимодействия, а, следовательно, увеличиваются плотность вещества, t°плавления и t°кипения.
 Сравнение ионной и ковалентной полярной связей Общее: образование общей электронной пары. Отличие: степень смещения общей электронной пары (поляризация связи). Ионную связь следует рассматривать как крайний случай ковалентной полярной связи.
Сравнение ионной и ковалентной полярной связей Общее: образование общей электронной пары. Отличие: степень смещения общей электронной пары (поляризация связи). Ионную связь следует рассматривать как крайний случай ковалентной полярной связи.
 Сравнение характеристик ионной и ковалентной полярной связей Ковалентная связь: насыщена и направлена Насыщаемость (максимальная валентность) - определяется способностью атома образовывать ограниченное количество связей (с учетом обоих механизмов образования). Направление связи задает валентный угол, зависящий от типа гибридизации орбиталей центрального атома. Ионная связь: ненасыщена и ненаправлена.
Сравнение характеристик ионной и ковалентной полярной связей Ковалентная связь: насыщена и направлена Насыщаемость (максимальная валентность) - определяется способностью атома образовывать ограниченное количество связей (с учетом обоих механизмов образования). Направление связи задает валентный угол, зависящий от типа гибридизации орбиталей центрального атома. Ионная связь: ненасыщена и ненаправлена.
 Сравнение характеристик ионной и ковалентной полярной связей Направленность связи задают валентные углы. Валентные углы определяют экспериментально или предсказывают на основе теории гибридизации атомных орбиталей Л. Поллинга либо теории Гиллеспи. Подробно об этом на семинарах.
Сравнение характеристик ионной и ковалентной полярной связей Направленность связи задают валентные углы. Валентные углы определяют экспериментально или предсказывают на основе теории гибридизации атомных орбиталей Л. Поллинга либо теории Гиллеспи. Подробно об этом на семинарах.
 Сравнение свойств веществ с ионными и ковалентными связями Ковалентные связи Атомные кристаллы Между атомами в самом кристалле Высокая твердость высокие tºплав, tºкип плохие тепло- и электропроводность Молекулярные кристаллы Между атомами в молекуле Умеренная мягкость достаточно низкие tº плав, tºкип плохие тепло- и Электропроводность Нерастворимы в воде
Сравнение свойств веществ с ионными и ковалентными связями Ковалентные связи Атомные кристаллы Между атомами в самом кристалле Высокая твердость высокие tºплав, tºкип плохие тепло- и электропроводность Молекулярные кристаллы Между атомами в молекуле Умеренная мягкость достаточно низкие tº плав, tºкип плохие тепло- и Электропроводность Нерастворимы в воде

 Сравнение свойств веществ с ионными и ковалентными связями Атомный ковалентный кристалл Температура плавления ≈ 3700 °С
Сравнение свойств веществ с ионными и ковалентными связями Атомный ковалентный кристалл Температура плавления ≈ 3700 °С
 Сравнение свойств веществ с ионными и ковалентными связями Ионные связи между ионами в кристалле твердость и хрупкость высокая температура плавления плохие тепло- и электропроводность Растворимы в воде
Сравнение свойств веществ с ионными и ковалентными связями Ионные связи между ионами в кристалле твердость и хрупкость высокая температура плавления плохие тепло- и электропроводность Растворимы в воде

 Металлическая связь осуществляется электронами, принадлежащими всем атомам одновременно. Электронная плотность делокализована «электронный газ» . Характерный металлический блеск Пластичность Ковкость Высокие тепло- и электропроводность Температуры плавления очень разные.
Металлическая связь осуществляется электронами, принадлежащими всем атомам одновременно. Электронная плотность делокализована «электронный газ» . Характерный металлический блеск Пластичность Ковкость Высокие тепло- и электропроводность Температуры плавления очень разные.
 Межмолекулярные связи. 1. Водородная связь Притяжение между атомом водорода (+) одной молекулы и атомом F, O, N (–) другой молекулы Полимер (HF)n Димер уксусной кислоты Водородные связи слабы индивидуально, но сильны коллективно
Межмолекулярные связи. 1. Водородная связь Притяжение между атомом водорода (+) одной молекулы и атомом F, O, N (–) другой молекулы Полимер (HF)n Димер уксусной кислоты Водородные связи слабы индивидуально, но сильны коллективно
 Межмолекулярные связи. 5. Ван-дер-ваальсовы связи Даже если между молекулами нет водородных связей, молекулы всегда притягиваются друг к другу. Притяжение между молекулярными диполями называют вандер-ваальсовой связью. В-д-в притяжение тем сильнее, чем больше: 1) полярность; 2) размер молекул. Пример: метан (CH 4) – газ, бензол (C 6 H 6) – жидкость Одна из самых слабых в-д-в связей – между молекулами H 2 (т. пл. – 259 о. С, т. кип. – 253 о. С). Взаимодействие между молекулами во много раз слабее связи между атомами: Eков(Cl–Cl) = 244 к. Дж/моль, Eвдв(Cl 2–Cl 2) = 25 к. Дж/моль но именно обеспечивает существование жидкого и твердого состояния вещества
Межмолекулярные связи. 5. Ван-дер-ваальсовы связи Даже если между молекулами нет водородных связей, молекулы всегда притягиваются друг к другу. Притяжение между молекулярными диполями называют вандер-ваальсовой связью. В-д-в притяжение тем сильнее, чем больше: 1) полярность; 2) размер молекул. Пример: метан (CH 4) – газ, бензол (C 6 H 6) – жидкость Одна из самых слабых в-д-в связей – между молекулами H 2 (т. пл. – 259 о. С, т. кип. – 253 о. С). Взаимодействие между молекулами во много раз слабее связи между атомами: Eков(Cl–Cl) = 244 к. Дж/моль, Eвдв(Cl 2–Cl 2) = 25 к. Дж/моль но именно обеспечивает существование жидкого и твердого состояния вещества
 В лекции использованы материалы профессора химического факультета МГУ им. Ломоносова Еремина Вадима Владимировича Спасибо за внимание!
В лекции использованы материалы профессора химического факультета МГУ им. Ломоносова Еремина Вадима Владимировича Спасибо за внимание!
Электроотрицательностью называется свойство химического элемента притягивать к своему атому электроны от атомов других элементов, с которыми данный элемент образует химическую связь в соединениях.
При образовании химической связи между атомами разных элементов общее электронное облако смещается к более электроотрицательному атому, из-за чего связь становится ковалентно-полярной, а при большой разности электроотрицательностей – ионной.
Электроотрицательность учитывается при написании химических формул: в бинарных соединениях сзади записывается символ наиболее электроотрицательного элемента.
Электроотрицательность возрастает в направлении слева направо для элементов каждого периода и уменьшается в направлении сверху вниз для элементов одной и той же группы ПС.
Валентностью элемента называется свойство его атомов соединяться с определенным числом других атомов.
Различают стехиометрическую, электронную валентность и координационное число. Мы рассмотрим только стехиометрическую валентность.
Стехиометрическая валентность показывает, сколько атомов другого элемента присоединяет атом данного элемента. За единицу валентности принята валентность водорода, т.к. водород всегда одновалентен. Например, в соединениях HCl, H 2 O, NH 3 (правильное написание аммиака Н 3 N уже используется в современных пособиях), СН 4 хлор одновалентен, кислород двухвалентен, азот трехвалентен и углерод четырехвалентен.
Стехиометрическая валентность кислорода обычно равна 2. Так как почти все элементы образуют соединения с кислородом, то удобно его использовать в качестве эталона для определения валентности другого элемента. Например, в соединениях Na 2 O, CoO, Fe 2 O 3 , SO 3 натрий одновалентен, кобальт двухвалентен, железо трехвалентно, сера шестивалентна.
В окислительно-восстановительных реакциях нам важно будет определять степени окисления элементов.
Степенью окисления элемента в веществе называется его стехиометрическая валентность, взятая со знаком плюс или минус.
Химические элементы подразделяются на элементы постоянной валентности элементы переменной валентности.
1.3.3. Вещества молекулярного и немолекулярного строения. Тип кристаллической решетки. Зависимость свойств веществ от их состава и строения.
В зависимости от того, в каком состоянии соединения находятся в природе, они делятся на молекулярные и немолекулярные. В молекулярных веществах мельчайшими структурными частицами являются молекулы. Эти вещества имеют молекулярную кристаллическую решетку. В немолекулярных веществах мельчайшими структурными частицами являются атомы или ионы. Кристаллическая решетка у них атомная, ионная или металлическая.
Тип кристаллической решетки во многом определяет свойства веществ. Например, металлы, имеющие металлический тип кристаллической решетки , отличаются от всех остальных элементов высокой пластичностью, электро- и теплопроводностью . Эти свойства, а также и многие другие – ковкость, металлический блеск и т.п. обусловлены особым видом связи между атомами металла -- металлической связью. Необходимо отметить, что свойства, присущие металлам, проявляются только в конденсированном состоянии. Например, серебро в газообразном состоянии не обладает физическими свойствами металлов.
Особый тип связи в металлах – металлическая – обусловлен дефицитом валентных электронов, поэтому они общие для всей структуры металла. Наиболее простая модель строения металлов предполагала, что кристаллическая решетка металлов состоит из положительных ионов, окруженных свободными электронами, движение электронов происходит хаотически, подобно молекулам газа. Однако такая модель, качественно объясняя многие свойства металлов, при количественной проверке оказывается недостаточной. Дальнейшая разработка теории металлического состояния привела к созданию зонной теории металлов , которая основывается на представлениях квантовой механики.
В узлах кристаллической решетки находятся катионы и атомы металла, а электроны свободно перемещаются по кристаллической решетке .
Характерным механическим свойством металлов является пластичность , обусловленная особенностями внутреннего строения их кристаллов. Под пластичностью понимают способность тел под действием внешних сил подвергаться деформации, которая остается и после прекращения внешнего воздействия. Это свойство металлов позволяет придавать им различную форму при ковке, прокатывать металл в листы или вытягивать в проволоку.
Пластичность металлов обусловлена тем, что при внешнем воздействии слои ионов, образующих кристаллическую решетку, сдвигаются относительно друг друга без разрыва. Это происходит в результате того, что переместившиеся электроны благодаря свободному перераспределению продолжают осуществлять связь межу ионными слоями. При механическом воздействии на твердое вещество с атомной решеткой смещаются отдельные ее слои и сцепление между ними нарушается из-за разрыва ковалентных связей.
ионы , то эти вещества образуют ионный тип кристаллической решетки .


Это соли, а также оксиды и гидроксиды типичных металлов. Это твердые, хрупкие вещества, но основное их качество: растворы и расплавы этих соединений проводят электрический ток .
Если в узлах кристаллической решетки находятся атомы , то эти вещества образуют атомный тип кристаллической решетки (алмаз, бор, кремний оксиды алюминия и кремния). По свойствам очень твердые и тугоплавкие, нерастворимы в воде.
Если в узлах кристаллической решетки находятся молекулы , то эти вещества образуют (при обычных условиях газы и жидкости: О 2 , HCl; I 2 органические вещества).
Интересно отметить металл галлий, который плавится при температуре 30 о С. Эта его аномалия объясняется тем, что в узлах кристаллической решетки находятся молекулы Ga 2 и его свойства в чем становятся схожи с веществами, имеющие молекулярную кристаллическую решетку.

Пример. Немолекулярное строение имеют все неметаллы группы:
1) углерод, бор, кремний; 2) фтор, бром, иод;
3) кислород, сера, азот; 4) хлор, фосфор, селен.
В немолекулярных веществах мельчайшими структурными частицами являются атомы или ионы. Кристаллическая решетка у них атомная, ионная или металлическая
При решении этого вопроса проще идти от противного. Если в узлах кристаллической решетки находятся молекулы , то эти вещества образуют молекулярный тип кристаллической решетки (при обычных условиях газы и жидкости: О 2 , HCl; также I 2, ромбическая сера S 8 , белый фосфор Р 4 , органические вещества). По свойствам это непрочные легкоплавкие соединения.
Во втором ответе есть газ фтор, в третьем – газы кислород, азот, в четвертом – газ хлор. Значит, эти вещества имеют молекулярную кристаллическую решетку и молекулярное строение.
В первом ответе все вещества – твердые соединения при обычных условиях и образуют атомную решетку, значит, имеют немолекулярное строение.
Правильный ответ: 1) углерод, бор, кремний
Для большинства веществ характерна способность в зависимости от условий находиться в одном из трех агрегатных состояний: твердом, жидком или газообразном.
Например, вода при нормальном давлении в интервале температур 0-100 o C является жидкостью, при температуре выше 100 о С способна существовать только в газообразном состоянии, а при температуре менее 0 о С представляет собой твердое вещество.
Вещества в твердом состоянии различают аморфные и кристаллические.
Характерными признаками аморфных веществ является отсутствие четкой температуры плавления: их текучесть плавно увеличивается с ростом температуры. К аморфным веществам относятся такие соединения, как воск, парафин, большинство пластмасс, стекло и т.д.
Все же кристаллические вещества обладают конкретной температурой плавления, т.е. вещество с кристаллическим строением переходит из твердого состоянии в жидкое не постепенно, а резко, при достижении конкретной температуры. В качестве примера кристаллических веществ можно привести поваренную соль, сахар, лед.
Разница в физических свойствах аморфных и кристаллических твердых веществ обусловлена прежде всего особенностями строения таких веществ. В чем заключается разница между веществом в аморфном и кристаллическом состоянии, проще всего понять из следующей иллюстрации:
Как можно заметить, в аморфном веществе, в отличие от кристаллического, отсутствует какой-либо порядок в расположении частиц. Если же в кристаллическом веществе мысленно соединить прямой два близкорасположенных друг к другу атома, то можно обнаружить, что на этой линии на строго определенных промежутках будут лежать одни и те же частицы:
Таким образом, в случае кристаллических веществах можно говорить о таком понятии, как кристаллическая решетка.
Кристаллической решеткой называют пространственный каркас, соединяющий точки пространства, в которых находятся частицы, образующие кристалл.
Точки пространства, в которых находятся образующие кристалл частицы, называют узлами кристаллической решетки .
В зависимости от того, какие частицы находятся в узлах кристаллической решетки, различают: молекулярную, атомную, ионную и металлическую кристаллические решетки .
В узлах молекулярной кристаллической решетки
Кристаллическая решетка льда как пример молекулярной решеткинаходятся молекулы, внутри которых атомы связаны прочными ковалентными связями, однако сами молекулы удерживаются друг возле друга слабыми межмолекулярными силами. Вследствие таких слабых межмолекулярных взаимодействий кристаллы с молекулярной решеткой являются непрочными. Такие вещества от веществ с иными типами строения отличаются существенно более низкими температурами плавления и кипения, не проводят электрический ток, могут как растворяться, так и не растворяться в различных растворителях. Растворы таких соединений могут как проводить, так и не проводить электрический ток в зависимости от класса соединения. К соединениям с молекулярной кристаллической решеткой относятся многие простые вещества — неметаллы (отвержденные H 2 , O 2 , Cl 2 , ромбическая сера S 8 , белый фосфор P 4), а также многие сложные вещества – водородные соединения неметаллов, кислоты, оксиды неметаллов, большинство органических веществ. Следует отметить, что, если вещество находится в газообразном или жидком состоянии, говорить о молекулярной кристаллической решетке неуместно: корректнее использовать термин — молекулярный тип строения.
Кристаллическая решетка алмаза как пример атомной решеткиВ узлах атомной кристаллической решетки
находятся атомы. При этом все узлы такой кристаллической решетки «сшиты» между собой посредством прочных ковалентных связей в единый кристалл. Фактически, такой кристалл является одной гигантской молекулой. Вследствие особенностей строения все вещества с атомной кристаллической решеткой являются твердыми, обладают высокими температурами плавления, химически мало активны, не растворимы ни в воде, ни в органических растворителях, а их расплавы не проводят электрический ток. Следует запомнить, что к веществам с атомным типом строения из простых веществ относятся бор B, углерод C (алмаз и графит), кремний Si, из сложных веществ — диоксид кремния SiO 2 (кварц), карбид кремния SiC, нитрид бора BN.
У веществ с ионной кристаллической решеткой
в узлах решетки находятся ионы, связанные друг с другом посредством ионных связей.
Поскольку ионные связи достаточно прочны, вещества с ионной решеткой обладают сравнительно высокой твердостью и тугоплавкостью. Чаще всего они растворимы в воде, а их растворы, как и расплавы проводят электрический ток.
К веществам с ионным типом кристаллической решетки относятся соли металлов и аммония (NH 4 +), основания, оксиды металлов. Верным признаком ионного строения вещества является наличие в его составе одновременно атомов типичного металла и неметалла.
 Кристаллическая решетка хлорида натрия как пример ионной решетки
Кристаллическая решетка хлорида натрия как пример ионной решетки
наблюдается в кристаллах свободных металлов, например, натрия Na, железа Fe, магния Mg и т.д. В случае металлической кристаллической решетки, в ее узлах находятся катионы и атомы металлов, между которыми движутся электроны. При этом движущиеся электроны периодически присоединяются к катионам, таким образом нейтрализуя их заряд, а отдельные нейтральные атомы металлов взамен «отпускают» часть своих электронов, превращаясь, в свою очередь, в катионы. Фактически, «свободные» электроны принадлежат не отдельным атомам, а всему кристаллу.
Такие особенности строения приводят к тому, что металлы хорошо проводят тепло и электрический ток, часто обладают высокой пластичностью (ковкостью).
Разброс значений температур плавления металлов очень велик. Так, например, температура плавления ртути составляет примерно минус 39 о С (жидкая в обычных условиях), а вольфрама — 3422 °C. Следует отметить, что в обычных условиях все металлы, кроме ртути, являются твердыми веществами.











